Das enorme Jahrestreffen der American Diabetes Association, genannt Scientific Sessions, fand in der vergangenen Woche im dampfenden Orlando statt. Mit ~ 16.000 Diabetesfachleuten, die sich an fünf Tagen treffen, um Hunderte von Präsentationen, Symposien, Forschungsplakaten und Strategietreffen zu teilen, sowie einer lebhaften Ausstellungshalle von der Größe eines Flugzeugbügels ist es schwierig, die Größe des weltweit größten Diabetesereignisses zu überschätzen. (Es genügt zu sagen, dass man mit einem müden Kopf und müden Füßen nach Hause geht.)

Die großen Diskussionsthemen, die wir in diesem Jahr aufgegriffen haben, waren Zugang und Erschwinglichkeit sowie eine Menge Forschung und Aufregung um neue Systeme mit geschlossenem Regelkreis. Außerdem war die DIY-Community der Patienten in einigen herausragenden Sitzungen stark vertreten, bis zu dem Punkt, an dem sie das Gefühl hatten, endlich als Partner aufgenommen zu werden, zumindest in den Augen einiger Gruppenleiter von Nightscout:

Woot!
ADAs neue Frauengruppe und mehr
Für die ADA haben sie ihre jüngsten Lobbyarbeit in Bezug auf Zugang und Erschwinglichkeit mit einem neuen Weißbuch angepriesen. Überwindung von Stigmatisierung und gesundheitlichen Ungleichheiten; und sich für Investitionen in die Forschung einzusetzen - mit ihrem Pathways-Programm als „alarmierend unterfinanziert“ bezeichnet - und eine # FundtheMission-Kampagne vorzuschlagen, die der im Krebsbereich durchgeführten ähnelt.
Die traditionelle „Banting Lecture“ (benannt nach dem Mitentdecker des Insulins), die dieses Jahr von der ADA-Präsidentin für Medizin und Wissenschaft, Dr. Jane Reusch, gehalten wurde, enthielt einen Aufruf an die HCPs, „die Geschichte zu kennen, die Geschichte zu erzählen“. Mit anderen Worten, jeder sollte es als seine persönliche Aufgabe betrachten, das Bewusstsein für die erforderliche Pflege und den Zugang zu Werkzeugen zu schärfen.
Reusch sprach auch ausführlich über den Diabetes Disaster Relief Fund der ADA angesichts der jüngsten Hurrikane, Brände und anderer Naturkatastrophen, auf die die Organisation reagieren musste.
Die größte Neuigkeit von ADA ist jedoch die Einrichtung des neuen Women's Interpersonal Network der American Diabetes Association (WIN ADA), eines Netzwerks nur für Mitglieder, das sowohl die Karrieren aller Frauen im Bereich Diabetes unterstützt als auch im Rampenlicht steht zur Erforschung des Geschlechts als biologischer Faktor für die Gesundheit von Frauen mit Diabetes.

Reusch plädierte auch für die Förderung des Closed-Loop- und CGM-Einsatzes bei Patienten und unterstrich damit eine neue Welle des Vertrauens in Technologie-Tools, die auf ihrer Prävalenz, ihrem Patienteninteresse und vielen neuen Daten basiert, die positive Ergebnisse zeigen!
Wir werden bald in den SciSessions zur Wissenschaft kommen, aber für heute: Was war genau an der Produktfront groß? Nun… Abbott Libre, Dexcom G6, das neue DASH-System von OmniPod, und eine ganze Reihe neuer Dinge, die in den Tagen vor der Konferenz plötzlich von der FDA genehmigt wurden.

FDA-Zulassung (!): Eversense, Basal IQ, InPen Insights
Eversense: Das neue implantierbare verbundene CGM-System von Senseonics war zweifellos die Schönheit des Balls auf dem Ausstellungsboden - denn es stellt eine völlig neue Kategorie von CGM dar und wurde erst am Freitag von der FDA zugelassen, als die Konferenz begann. Hier finden Sie unsere vollständige Abdeckung dieses Produkts / dieser Zulassung. Die Kabine wurde jeden Tag so stark überflutet, dass es manchmal schwierig war, eine Spitze des Prothesenarms zu erreichen, mit dem die Sensoreinführung demonstriert wurde.


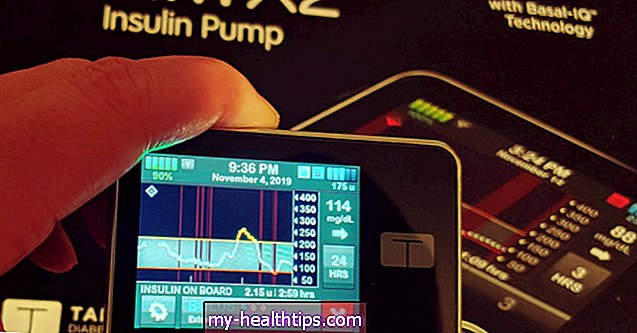
Tandem: Man könnte sagen, dass Tandem Diabetes Care nach Gerüchten über ihren Tod ein atemberaubendes Comeback feierte. Sie hatten einen großen Stand vorne und in der Mitte in der Nähe des Haupteingangs der Ausstellungshalle und zeigten stolz ihre gerade von der FDA genehmigte Basal-IQ-Technologie, eine prädiktive PLGS-Funktion (Low Glucose Suspension) für ihren t: slim X2 Insulinpumpe, die über Dexcom G6 funktioniert (ja, das neueste Modell!). Natürlich soll es dazu beitragen, die Häufigkeit und Dauer von Hypoereignissen zu reduzieren und die Insulinabgabe zu unterbrechen, wenn der Blutzuckerspiegel voraussichtlich unter 80 mg / dl fällt oder wenn der Blutzuckerspiegel derzeit unter 70 mg / dl liegt und sinkt.
Das Besondere an dieser Funktion zur Suspendierung niedriger Glukose ist jedoch, dass sie konstant und dynamisch ist. Dies bedeutet, dass das System das Insulin sofort wieder aufnimmt, sobald die BG-Werte zu steigen beginnen, anstatt die Abgabe für einen festgelegten Zeitraum automatisch zu stoppen. Daher wird die Lieferung möglicherweise mehrmals täglich oder sogar noch häufiger für einige Momente vorübergehend unterbrochen, bis Sie wieder in Reichweite sind. Benutzer können wählen, ob jedes Mal Warnungen ausgegeben werden sollen, obwohl diese Verwaltungsfunktion im Hintergrund arbeiten soll, damit wir PWDs weniger Sorgen machen müssen (!) Tandem plant, Basal-IQ zu starten im August mit aktuellen t: schlanken Pumpen ein kostenloses Upgrade erhalten; Das Unternehmen bestimmt weiterhin, welche Upgrade-Optionen es denjenigen bietet, die noch das Dexcom G5-Modell verwenden.
Auf Wiedersehen, t: flex: ICYMI, Tandem hat seine größere t: flex-Insulinpumpe mit 480 Einheiten eingestellt, weil die Nachfrage nicht ausreichte, um eine Verlängerung zu rechtfertigen. Ab Ende Juni ist dieses Gerät nicht mehr für Neukunden verfügbar. Das Unternehmen plant jedoch, bis zum Ablauf der Garantiezeit weiterhin Verbrauchsmaterialien für aktuelle Benutzer bereitzustellen.

InPen: Ebenfalls erst am Freitag von der FDA zugelassen wurde Companion Medicals Insights by InPen - der Datenteil der App, der mit ihrem coolen neuen Smart Pen kombiniert wird. Letztes Jahr war das InPen-System der einzige von der FDA zugelassene intelligente Insulinstift mit einer Diabetes-Management-App, mit der Stiftbenutzer beginnen konnten, Dosen zu verfolgen und die Art von Daten zu sammeln, die bisher nur Pumpern zur Verfügung standen. Die umfassende Insights-App enthält jetzt die durchschnittliche Glukose, die durchschnittliche tägliche Gesamtdosis, die Verwendung des Dosisrechners, verpasste Dosen und detaillierte Tagesansichten. Das Unternehmen nennt dies einen Meilenstein, der die Landschaft verändern wird, da es bisher unmöglich war, Daten von MDI-Patienten (tägliche Insulin-Shots) auf diese Weise zu verfolgen. Dies könnte sogar neue nationale Forschungsergebnisse zu den Gewohnheiten und Ergebnissen von Stiftbenutzern liefern, heißt es.

DreaMed: Eine weitere FDA-Zulassung in der Produktpalette war die Genehmigung für DreaMed Diabetes aus Israel, die DreaMed Advisor Pro-App zur Optimierung der Insulinpumpeneinstellungen zu vermarkten. Sie erinnern sich vielleicht an DreaMed als eines von mehreren Unternehmen, das Algorithmen mit geschlossenem Regelkreis für ein eventuelles künstliches Pankreas-System entwickelt. Jetzt haben sie einen Teil ihrer Technologie als "Cloud-basierte digitale Lösung" zusammengefasst, die Empfehlungen zur Insulinabgabe generiert, indem sie Informationen aus CGM, selbstüberwachenden Blutzuckerwerten (SMBG) und Insulinpumpendaten analysiert und ereignisgesteuertes adaptives Lernen anwendet. Es verwendet AI, um „sein Verständnis für jeden Einzelnen zu verfeinern und Empfehlungen an den Gesundheitsdienstleister zu senden, wie die Insulinpumpeneinstellungen eines Patienten hinsichtlich Basalrate, Kohlenhydratverhältnis (CR) und Korrekturfaktor (CF) optimiert werden können.“ Im Vorgriff auf dieses Angebot hatten sie bereits eine Vereinbarung mit dem D-Data-Plattform-Anbieter Glooko über die Integration des Advisor Pro-Tools in diese Plattform unterzeichnet. Eine sehr coole Anwendung künstlicher Intelligenz in der Diabetesversorgung und eine großartige Option für Pumpen, die Glooko verwenden!
Abbott Libre
Das Abbott Libre Flash-Glukoseüberwachungssystem (im September letzten Jahres für den Verkauf in den USA zugelassen) war mit seiner Präsentation im Product Theatre und einem überfüllten Stand zweifellos ein Star für sich. Dieses neue System ist „werkseitig kalibriert“, sodass keine Fingerstick-Kalibrierungen erforderlich sind. Es ist zu geringeren Kosten erhältlich. Eine vorgestellte Studie ergab, dass Menschen, die Libre verwenden, durchschnittlich 120 US-Dollar weniger pro Monat ausgeben, ohne Teststreifen kaufen zu müssen.
In Bezug auf die Ergebnisse veröffentlichte das Unternehmen Ergebnisse einer kombinierten Analyse von 17 früheren Studien, aus denen hervorgeht, dass Benutzer eine durchschnittliche Reduzierung der A1C um 0,56 Punkte hatten und deutlich mehr Zeit in Reichweite verbrachten. Interessanterweise stammen diese Daten von 250.000 nicht von Abbott rekrutierten „realen“ Patienten, die sich über Typ 1, Typ 2 und verschiedene Altersgruppen, einschließlich Teenager und junge Erwachsene, erstrecken.
In einer Erklärung sagte Abbotts Direktor für klinische und rechnergestützte Forschung, Tim Dunn: "Auf der Ebene der Glukosekontrolle sehen wir eine wirklich starke Beziehung zwischen Menschen, die ihre Glukose häufiger überprüfen, und ihrer Kontrolle."
Sie teilen uns mit, dass FreeStyle Libre derzeit von mehr als 650.000 Menschen in mehr als 42 Ländern verwendet wird und dass Abbott in 28 Ländern, darunter Frankreich, Irland, Japan und Großbritannien, eine teilweise oder vollständige Erstattung des Systems sichergestellt hat.
Ein Knackpunkt (kein Wortspiel beabsichtigt) ist die Tatsache, dass die USA noch auf die Genehmigung der LibreLink-App warten, dem Datenmanager für dieses System. Immer noch kein Wort über den genauen Zeitpunkt.
Dexcom

Das Unternehmen zeigte sein neuestes G6-Modell mit einem flacheren Sensor, erhöhter Genauigkeit, Warnmeldungen für niedrige und hohe Vorhersagen und einer neu gestalteten Begleit-Telefon-App. Tatsächlich sagt uns CEO Kevin Sayer: „G6 unterscheidet sich grundlegend von früheren Produkten - den Membranen, Teilen und Algorithmen. Wir haben alles verändert. “
Sie waren begeistert, dass G6 die neue „iCGM-Kategorie“ der FDA verlassen konnte, was eine schnellere Anmeldezeit ermöglichte. Auf die Frage nach der Herausforderung, die Marktnachfrage zu befriedigen, sagte er: "Wir sind jetzt auch zehnmal größer als beim Start der G4" (als es ursprünglich zu Verzögerungen beim Versand kam).
Auf die Frage nach anderen Herausforderungen gab Sayer zu: „Wir haben Probleme mit der Übertragungsreichweite und mit Verbindungslücken. Wir haben das Gerät so konzipiert, dass Bluetooth zwischendurch ausgeschaltet wird, um die Lebensdauer des Sensors zu verlängern und den Akku zu schonen. (Aber) wir müssen das System jetzt neu konstruieren, damit Bluetooth-Lücken verschwinden. “ Einverstanden!
Dennoch sagt Sayer, dass sie in zukünftigen Generationen in der Lage sein werden, die Notwendigkeit eines Empfängers vollständig zu beseitigen, noch bevor sie die Bluetooth-Probleme vollständig lösen.
Er sagt im Moment, es sind "alle Hände an Deck mit der G6, und das wird als nächstes in Europa eingeführt." Dann wird es G6-Derivate geben (inkrementelle Upgrades), gefolgt von einer vollständig verfügbaren Plattform, der G7. “ Letzteres ist Teil ihrer Arbeit mit Verily, die mehr T2- und verbraucherorientierte CGMs entwickelt.
„Im Moment kosten die Sensoren zu viel, um weggeworfen zu werden“, sagt er. Das erste Produkt, das sie mit Verily auf den Markt bringen, basiert auf dem G6, aber „kleiner und einfacher für die Leute zu bezahlen… und nur für den Sensor , mit weniger Funktionalität und 14-tägigem Verschleiß. “
Sie möchten auch eine KI einbauen, die die Gewohnheiten der Benutzer lernt und die Einstellungen entsprechend anpassen kann. Er würde die Anpassung gerne als "Ich möchte jetzt ins Bett gehenSchaltfläche, mit der das System Ihre Schlafeinstellungen aktivieren kann.
Was ist mit dem neuen Wettbewerb, fragten wir? „Libre hat unseren Fokus erhöht und das Bewusstsein für CGM insgesamt geschärft. Es hat uns dazu gebracht, schneller zu denken und voranzukommen und den Markt zu erweitern. Wenn es Auswirkungen auf irgendetwas hat, wäre es die Preisgestaltung. Wir müssen uns fragen, was können wir zu welchem Preis bauen? Wir möchten ein umfassenderes Dexcom-Produkt zu einem Libre-Preis. “
Gut zu wissen!
OmniPod DASH
Insulet, Hersteller der beliebten schlauchlosen Omnipod-Pumpe, freute sich über das auffällige Display ihrer neuen DASH-Plattform, die erst am 4. Juni von der FDA zugelassen wurde.
- Telefon-Touchscreen mit einfachem Bildlauf im Gegensatz zum manuellen Tastendruck auf dem alten PDM, bei dem Sie beispielsweise durch das gesamte Alphabet tippen müssen, um ein neues Basalprogramm festzulegen
- IOB (Insulin an Bord) wird auf dem Homescreen angezeigt
- verfügt über eine verbesserte Food-Datenbank basierend auf FoodKing mit 80.000 Artikeln
- Software kann drahtlos aus der Ferne aktualisiert werden
- Ermöglicht das Duplizieren und Kopieren von Basalratenmustern und das Einstellen von Basalraten mit 0 Einheiten nach Bedarf
- Möglichkeit zur manuellen Eingabe von BG- und anderen Daten sowie zur Personalisierung von Essenseinträgen für den schnellen Zugriff
Insulet veranstaltete eine Abendveranstaltung bei ADA mit einem DASH-Benutzerpanel, bei der wir erfuhren, wie viel Patientenfeedback in die Entwicklung dieses neuen Systems floss. Ein großes Lob an dieses Unternehmen für die Einrichtung eines vollständigen „Labors“ für die gemeinsame Gestaltung mit Benutzern!
Zu Ihrer Information für Omnipod-Fans: Das neue System weist zwei Nachteile oder zumindest Änderungen auf.
- Erstens enthält der neue Android-Controller kein eingebautes Fingerstick-Messgerät mehr, was vielen gefallen hat, da kein zusätzliches Gerät mehr mitgeführt werden muss.
- Zweitens benötigt das neue System Lithium-Ionen-Batterien, die aufgeladen werden müssen, da es sich im Wesentlichen um ein Mobiltelefon handelt. Es ist also so, als hätte man ein anderes Telefon, das regelmäßig aufgeladen werden muss.
Abgesehen davon freuen wir uns sehr über das DASH-System, das die Verwendung des Omnipod-Systems noch einfacher macht und eindeutig ein Sprungbrett für ein eventuelles System ist, das direkt von Ihrem Smartphone aus gesteuert wird, ohne dass ein separates Gerät erforderlich ist.
Medtronic
Wie üblich hatte Medtronic eine gigantische Ausstellungskabine, die ständig voller Aktivitäten war. Sie waren ziemlich stolz darauf, dass der Medtronic 670G (erstmals im September 2016 zugelassen und letztes Jahr auf den Markt gebracht) am 21. Juni im Alter von 7 bis 13 Jahren endgültig von der FDA für den pädiatrischen Einsatz zugelassen wurde. Das Unternehmen zeigte auch sein eigenständiges Guardian Connect CGM, das erst kürzlich nach behördlicher Genehmigung Anfang des Jahres eingeführt wurde.
Sugar.IQ: Zusammen mit dem eigenständigen CGM hat Medtronic die mobile Sugar.IQ-App „Diabetes Assistant“ eingeführt, die aus der IBM Watson-Partnerschaft stammt. Diese App mit KI-Unterstützung analysiert kontinuierlich, wie der Glukosespiegel der Benutzer auf die Nahrungsaufnahme, Insulindosierungen, tägliche Routinen und andere Faktoren reagiert, um Muster aufzudecken, die PWDs dabei helfen können, ihren Glukosespiegel im Zielbereich zu halten. Derzeit ist die App nur für iOS-Telefone verfügbar und kann nur mit Guardian Connect CGM und Insulininjektionstherapie verwendet werden. Das Unternehmen plant, es in naher Zukunft auch seinen Pumpenkunden anzubieten.
Nutrino Foodprint: Medtronic zeigte auch eine neue mobile App-Funktion, die sich auf Ernährung konzentriert und Foodprint genannt wird und aus einer Partnerschaft mit dem Startup Nutrino stammt. Benutzer können ihre Lebensmittel protokollieren, indem sie ein Foto von jedem Snack oder jeder Mahlzeit machen. Das AI-gestützte Programm vergleicht jeden Lebensmitteleintrag mit den CGM-Daten nach der Mahlzeit. Alle 6 Tage wird die App mit allen D-Daten synchronisiert, um einen "Foodprint" -Report zu erstellen, der den Glukosespiegel, die Zeitspanne und die Muster anzeigt.
Derzeit ist Foodprint nur als Funktion der iPro2 MyLog-App in Verbindung mit der für HCPs spezifischen verblindeten CGM-Version verfügbar. Das Unternehmen teilt uns jedoch mit, dass es in Kürze auch für die Verwendung in seiner Sugar.IQ-App für Guardian Connect- und Minimed 670G-Systeme sowie für zukünftige D-Geräte angeboten wird.
Beachten Sie, dass im Foodprint-Bericht jeder protokollierten Mahlzeit des Benutzers eine Briefnote von A bis F zugewiesen wird, basierend auf den Glukosewerten nach der Mahlzeit. Eine Mahlzeit, die BG versetzt hat, könnte also ein D oder F erhalten. "Die Absicht ist es, die Reaktion einer Person auf Lebensmittel zu verstehen und eine aussagekräftige Diskussion über diese Ergebnisse zu führen", sagt das Unternehmen.

Einige Leute wiesen jedoch darauf hin, dass dieses Bewertungssystem dem Schämen von Lebensmitteln ähnelt, da es den Menschen das Gefühl gibt, beurteilt zu werden, was sie essen möchten. Die Idee ist, dass dieses Foodprint-Bewertungssystem angesichts der Tatsache, dass die Anzeige der BG-Werte als „gut“ oder „schlecht“ zurückgedrängt wird, möglicherweise nicht funktioniert.
Es wird interessant sein zu sehen, wie Benutzer reagieren, wenn diese App an Zugkraft gewinnt.
Tidepool-Datentests: Wir konnten nicht anders, als zu lächeln, als wir unsere Freunde bei der Open-Source-Datenorganisation Tidepool vor Ort bei ADA sahen. Wir freuten uns über die Ankündigung, dass die Datenaustauschplattform des gemeinnützigen Unternehmens jetzt Beta-Test-Unterstützung für Medtronic 630G bietet , 640G- und 670G-Geräte. Sie rekrutierten aktiv Benutzer der Medtronic 6-Serie, die zufällig bei ADA waren, um es auszuprobieren und ihre D-Geräte am Tidepool-Stand anzuschließen!
Mannkinds Afrezza
Mannkind war mit einem Stand für das inhalierte Insulin Afrezza im Haus, und als Benutzer selbst sieht unser Team immer gerne den riesigen Dreamboat-Inhalator an der Ausstellungswand. Viel mehr Konferenzteilnehmer schienen mit Afrezza viel vertrauter zu sein, als wir uns in den vergangenen Jahren erinnern.

In diesem Jahr zeigte Mannkind positive Studienergebnisse aus seinen STAT- und AFFINITY-Studien, in denen eine verbesserte Reichweite und eine verringerte Hypoglykämie untersucht wurden. Die STAT-Studie umfasste 60 Typ-1-Patienten und ist die erste randomisierte, kontrollierte Studie, in der CGM mit Afrezza angewendet wurde. Im Vergleich zu injiziertem Insulin und unter Verwendung von „zusätzlichen Dosen“ 1 und / oder 2 Stunden nach der Mahlzeit bietet Afrezza:
- Deutlich verbesserte ganztägige Glukosezeit im Bereich um durchschnittlich 1,5 Stunden oder 12%
- Deutlich verringerte Glukosevariabilität am Tag um 17%
- Reduzierte die Zeit, die bei Hypoglykämie verbracht wurde (d. H. <70 mg / dl), signifikant um 41% oder ungefähr 23 Minuten pro Tag
Die AFFINITY-Studie, auch mit Typ 1, zeigte, dass Afrezza im Vergleich zu injiziertem Insulinaspart:
- Senkt die Hypoglykämierate bei T1D signifikant und bietet gleichzeitig eine ähnliche oder bessere Blutzuckerkontrolle (54,1 Ereignisse pro Proband gegenüber 78,2 Ereignissen pro Proband, eine Verringerung um 31%).
- Zeigt im Durchschnitt 26% weniger Hypoglykämie über einen Bereich von HbA1c-Spiegeln, was den gleichen Grad an Blutzuckerkontrolle mit weniger Hypoglykämie als Insulinaspart ermöglicht
Dies ist natürlich genau die Art von Beweis, die das Unternehmen benötigt, um das Vertrauen der Anbieter und damit die Verschreibungen zu stärken.
In der Zwischenzeit hat das Unternehmen eine begrenzte TV-Werbekampagne gestartet und am 27. Juni (gestern) ein Investor- und Analystentreffen in New York City veranstaltet. Vor einigen Monaten veranstalteten sie auch eine Diabetes-Blogger-Veranstaltung, die ihnen eine gute Berichterstattung in der DOC-Patientengemeinschaft brachte (unser Team konnte nicht teilnehmen, aber wie bereits erwähnt, verwenden wir Afrezza selbst).
Mehr von der ADA Expo Floor
Natürlich gab es bei dieser großen Konferenz auch andere CGM-Möchtegern - obwohl derzeit zumindest seit einigen Jahren keine in den USA auf den Markt kommt.
EOFLOW ist ein in Korea ansässiges Unternehmen, das eine Omnipod-Patchpumpe sowie ein Dexcom CGM und einen telefonbasierten App-Controller entwickelt. Sie sagen uns, dass sie mindestens ein Jahr vor Abschluss des Studiums frei haben, planen jedoch, 2019 in den USA eine 1.0-Version mit einem größeren CGM-Sensor auf den Markt zu bringen und dann auf eine elegante runde Festplattenversion zu aktualisieren, die dem Misfit-Aktivitäts-Tracker ähnelt . Das System wird eine Funktion zur Suspendierung niedriger Glukose haben (die wahrscheinlich in Kürze bei allen Combo-Systemen zum Standard wird), und schließlich werden sie mit zukünftigen Closed-Loop-Funktionen für die Insulindosierung erweitert. Dieses Unternehmen ist ziemlich davon überzeugt, dass sein System Vorteile gegenüber bestehenden Produkten hat, wie diese Vergleichstabelle zeigt.
Glutalor, ein Medizintechnikunternehmen aus Pennsylvania, das ein System namens iWel Mobile CGM entwickelt, haben wir bereits auf dieser Konferenz gesehen und sie haben ihr System wieder vorgeführt. Dies sieht auch aus wie ein OmniPod-Patch mit einem kleinen Knopf oben zum Einfügen. Es werden Messwerte für 7 Tage direkt an ein Smartphone gesendet, um Anzeigen, Warnungen usw. zu erhalten. Obwohl dies interessant ist, wird uns bereits zum dritten Mal in Folge mitgeteilt, dass es noch keine ETA zum Start in den USA gibt.
Insulinhersteller:
Interessanterweise waren die drei großen Insulinhersteller - Lilly, Novo und Sanofi - auf dem Boden der Ausstellungshalle nicht mehr so sichtbar wie traditionell. Während Sanofi mit seinem Firmennamen in großen Buchstaben eine dominierende Präsenz hatte, waren Novo und Lilly bei Marketing-Displays mit Produktmarken subtiler.
Insbesondere kündigte Sanofi seine Pläne der nächsten Generation an, mit Verily (ehemals Google Life Sciences) und Sensile Medical in New Jersey zusammenzuarbeiten, um eine All-in-One-Insulinpflasterpumpe zu entwickeln - ähnlich wie Lilly Ende 2017 mit seiner Pipeline angekündigt hatte für eine Hybrid-Patch-Tubed-Pump- und Pen-Technologie. Sanofi sagt, dass sie sich auf Typ-2-Diabetes konzentrieren, und es gibt derzeit kein Wort über das Timing.
Wir haben auch festgestellt, dass im Gegensatz zur SciSessions-Konferenz 2017 keiner der Insulinhersteller in seinen Displays auf das Problem des Zugangs / der Erschwinglichkeit hingewiesen hat - obwohl dies ein riesiger Elefant im Raum ist. Stattdessen hatten die Pharmaunternehmen das Thema, über Insulin hinauszugehen (sowohl Typ 2 als auch Typ 1) und ihre anderen Nicht-Insulin-Medikamente zu verwenden, um Therapien besser zu ergänzen.
Ein großer Stand mit dem Titel „Gehen Sie mit Typ-1-Diabetes über Insulin hinaus”Wurde von Sanofi unterstützt, der vermutlich den Markt für sein neues Medikament Sotagliflozin, den Markennamen Zynquista, ankurbelte, das derzeit von der FDA geprüft wird.
Es ist ein neues SGLT-1 / SGLT-2-Medikament, das gemeinsam von Lexicon Pharmaceuticals und Sanofi entwickelt wurde. Im Falle einer Zulassung wird Zynquista das erste orale Antidiabetikum sein, das in den USA für die Anwendung bei Erwachsenen mit Typ-1-Diabetes in Kombination mit Insulin (!) Zugelassen ist. Die Entscheidung der FDA zu Sotagliflozin wird am 22. März 2019 erwartet.

Es gab keine formelle Erwähnung dieses Medikaments am Stand, aber wir verstehen, dass am Sonntag Versuchsdaten vorgelegt wurden, die eine längere Reichweite zeigen.
Systeme mit geschlossenem Regelkreis:
Keines der kleineren Unternehmen, die Systeme mit geschlossenem Regelkreis entwickelten (Beta Bionics, Bigfoot usw.), hatte einen Stand auf der ADA, aber natürlich waren alle Teams anwesend. Mehrere Studien, die positive Ergebnisse zeigten, wurden zu viel Fanfare veröffentlicht, einschließlich einer Pressekonferenz am Samstag. Das in Frankreich entwickelte Diabeloop-System erhielt viel Aufmerksamkeit für seine internationale Studie, die zeigte, dass „ein leistungsstarkes und anpassbares Algorithmus-System für die Typ-1-Diabetes-Behandlung es Patienten ermöglichen kann, ihren Glukosespiegel signifikant und dauerhaft zu senken, ohne dass hypoglykämische Ereignisse zunehmen.“
Der CEO von Diabeloop, Erik Huneker French, spricht von anpassbar und erklärt, dass sein System nur von PWDs dynamisch und inkrementell erstellt wird. Zum Beispiel haben sie gerade eine einzigartige Funktion namens "Zen-Modus" hinzugefügt, um Ihr CGM nach dem Essen zu beruhigen, wenn Sie wissen, dass Sie für einen bestimmten Zeitraum hoch sein werden und keine Warnungen wünschen oder benötigen.

Insulintitrationswerkzeuge:
Neue technische Tools, mit denen Menschen ihre Insulindosierung optimieren können, sind ein wachsender Bereich! Abgesehen von den oben beschriebenen neuen Angeboten von DreaMed und Inpen haben wir Folgendes festgestellt:
Glytec, der in Massachussetts ansässige Anbieter von Tools zur Optimierung des Insulinmanagements im Krankenhaus und jetzt im ambulanten Bereich, hatte einen beträchtlichen Stand und warb für viele beeindruckende neue Fortschritte. Zum einen haben sie gerade das iGlucose-fähige Smart Meter zur Sammlung von Geräten hinzugefügt, mit denen ihre Software kompatibel ist. Ihr Krankenhaussystem hat eine signifikante Verringerung der hypoglykämischen Ereignisse und einen besseren Übergang zur Insulintherapie außerhalb des Krankenhauses gezeigt - alles gut! (Haftungsausschluss: „Die Minenredakteurin Amy Tenderich sitzt im Beirat von Glytec)
Mellitus Health hat ein ziemlich neues Angebot, um Ärzten bei jeder Einstellung zu helfen, Insulindosen besser zu titrieren. Das in Los Angeles ansässige Unternehmen wurde von Dr. Mayer Davidson, ehemaliger Präsident der ADA und ADA Physician Clinician of the Year 2016, gegründet und nimmt die berühmte Dr. Anne Peters von USC in sein Medical Board auf. Wir sind Gold wert. Die Plattform bietet Protokolle für 125 verschiedene Kombinationen von Insulintherapien. Daten, die einen positiven Effekt auf die A1C-Spiegel zeigen, wurden dieses Jahr auf der ADA vorgestellt.
Voluntis, Hersteller der Insulia-Plattform für Insulinmanagement, hatte auch einen kleinen Stand, der gut besucht war. Insulia ist eine App, die Insulindosisempfehlungen und pädagogische Coaching-Nachrichten als Reaktion auf BG-Werte bereitstellt, die in das Livongo-Messgerät, die WellDoc-App und andere integriert sind. Sie haben gerade eine Partnerschaft mit Monarch Medical Technologies angekündigt, um Insulia in ihr EndoTool-System zu integrieren, eine von der FDA zugelassene Software-Suite für präzise Empfehlungen zur stationären und ambulanten Insulindosierung.

Ernährungswerkzeuge:
Whisk sorgte als Gewinner des globalen Innovationswettbewerbs der Ascensia Diabetes Challenge für Aufsehen, der bei unserem Technologie-Event # Ddata18 am Freitag erstmals angekündigt und in der Vorschau gezeigt wurde. Whisk ist eine "kulinarische Coach" -App, die auf einem künstlichen intelligenten "Digital Dietician" basiert und derzeit für Verbraucher in Großbritannien und den USA verfügbar ist. Der Digital Dietician kombiniert Faktoren wie die persönlichen Geschmackspräferenzen der Benutzer, zeitliche Einschränkungen, Ziele, Budgets, diätetische Einschränkungen und Allergien, um die auf die Ernährung zugeschnittenen Rezepte vorzuschlagen. Die Plattform stellt dann eine direkte Verbindung zu den Online-Einkaufsplattformen einiger der weltweit führenden Lebensmitteleinzelhändler her, sodass Sie die Zutaten für das ausgewählte Rezept direkt in Ihren Online-Warenkorb legen können, um sie zu kaufen. Ascensia plant, mit Whisk zusammenzuarbeiten, um eine Version zu erstellen, die mit BG-Daten verknüpft ist, um maßgeschneiderte Rezeptempfehlungen für Menschen mit Diabetes zu erstellen, die auf ihre eigenen BG-Trends optimiert sind. Ziemlich cool!
Palette, ein weiteres Startup, das eine innovative Lebensmittelplattform schafft, war mit einem kleinen Stand auf der ADA vertreten. Es wird als "GPS für die Gesundheit" bezeichnet und verwendet ein sprachgesteuertes intelligentes Tischset (Palette), das die Ernährung Ihrer Mahlzeiten genau verfolgt. Es kommuniziert mit einer App, die Ihre Informationen verwendet, um personalisierte Empfehlungen zu erstellen, die auf Ihrer Ernährungsgeschichte, Ihrem Gesundheitszustand, Ihren körperlichen Eigenschaften und Ihren Lebensmittelpräferenzen basieren. Benutzer können auch ihre persönlichen Ernährungs- und Verhaltensziele, Medikamente und Kontakte von Anbietern und Betreuern verfolgen. Benutzer erhalten sofortiges Feedback zu aufgezeichneten Fortschritten und können auf Wunsch mit Anbietern, Betreuern und Familienmitgliedern über Nährwertinformationen und die Erstellung von Rezepten interagieren.
Und doch…
Trotz all dieser Fortschritte, Aufregung und klinischen Daten, die die Auswirkungen der Technologie belegen, scheint es Amerikanern mit Diabetes laut Dr. Joseph Wolfsdorf in seinem Vortrag während des „Joint ADA / ISPAD Symposium“ 25 Jahre später insgesamt weiterhin schlecht zu gehen die Bekanntgabe der DCCT-Ergebnisse - Wie ist der Status von Typ-1-Diabetes in der Jugend und wie können wir es besser machen? “

Grrr…