Eine neue Generation von inhaliertem Insulin nähert sich dem Markt, da sich ein wenig bekanntes biopharmazeutisches Unternehmen auf die späte klinische Forschung und die Einreichung durch die FDA vorbereitet und gerade einen erfahrenen CEO beauftragt hat, die Vermarktungsbemühungen zu leiten.
Sie erinnern sich vielleicht an Dance Biopharm, das Startup aus der Region San Francisco, das ungefähr 2010 auf den Markt kam, nachdem Pfizers gescheitertes Exubera-Inhalationsinsulin im Bong-Stil vom Markt genommen worden war und sich MannKinds Afrezza noch in der Entwicklung befand. Dieses Startup arbeitet seit fast einem Jahrzehnt daran, eine völlig neue Art von inhaliertem Insulin zu entwickeln.
Das Unternehmen macht jetzt Schlagzeilen mit der kürzlich erfolgten Einstellung der ehemaligen Sanofi-Managerin Anne Whitaker, die mit dem Universum für inhaliertes Insulin und der geschäftlichen Seite der Markteinführung neuer Medikamente bestens vertraut ist. Sie lebt in North Carolina, wo Dance Biopharm sich tatsächlich darauf vorbereitet, sein Hauptquartier in den kommenden Monaten zu verlegen. Sie werden an der Westküste bleiben, um Nachforschungen anzustellen, aber die Führungskräfte werden an der Ostküste sein, während Dance sich auch darauf vorbereitet, in Kürze Büros in China und England zu eröffnen.
„Wir waren vom Radar verschwunden, man könnte sagen, wir haben im Stealth-Modus gearbeitet. Aber wenn Sie sich die erzielten Fortschritte ansehen, ist dies bemerkenswert. All diese Dinge kommen zusammen… jetzt ist die Zeit gekommen, dies voranzutreiben “, sagt Whitaker über ihr neuartiges Produkt, das derzeit als Dance 501 (der interne Arbeitsname) bezeichnet wird.
In einem kürzlich durchgeführten Telefonat gab Whitaker uns Auskunft darüber, warum sie dem Dance-Team beigetreten ist und was wir in den nächsten Jahren erwarten können. Schauen wir uns zunächst dieses neue inhalierte Insulin an und welche Vorteile es für Patienten bietet.
Sizing Up Dance 501, auch bekannt als Inhaled Insulin 3.0
Die FDA wird alle vorgeschlagenen Produktmarken für dieses neue inhalative Insulin, das einige als Generation 3.0 bezeichnen, prüfen und genehmigen. Hier ein Blick auf die Eigenschaften von Dance 501:

Weicher Nebel: Im Gegensatz zu Afrezza-Insulin von MannKind, einem inhalierbaren weißen Pulver, ist Dance 501 eine Nebelformulierung, dh ein ultrakonzentriertes rekombinantes Insulin, das nur wenige Tropfen benötigt, die in Nebelform verdampft werden, wenn Sie es tief in die Lunge einatmen ein kleines Handgerät.
Rein: Im Gegensatz zu anderen Insulinen ist dieses Produkt frei von Konservierungsstoffen, was für 1-2% der PWDs wichtig ist, die tatsächlich eine Insulinallergie haben. Dies führt zu Problemen, die von Hautausschlägen an der Insulinstelle bis zu anaphylaktischem Schock reichen. Es wird in flüssiger Form in einer kleinen Flasche geliefert, mit der das Handgerät unmittelbar vor jeder Dosis gefüllt wird.
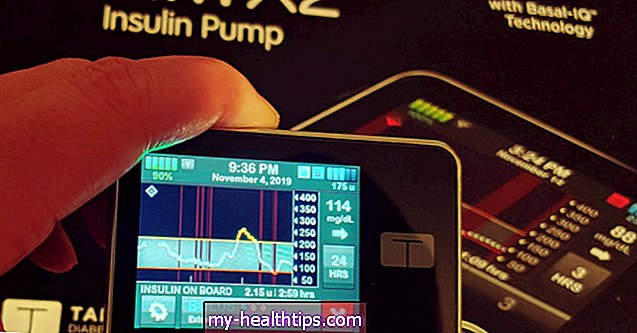
Handinhalator: Klein und einfach zu bedienen, ungefähr so groß wie ein Old-School-Piepser, der in eine Hosentasche passt. Dies ist ganz anders als bei frühen Prototypen, die wir gesehen haben. Im Dezember 2017 hat sich das Unternehmen mit dem Industriedesigner Phillips-Medisize für eine überarbeitete Version zusammengetan. Das Ergebnis ist ein elektronischer Inhalator, der die patentierte Vibrationsnetztechnologie verwendet, um gleich große Partikel von flüssigem Insulin in Form eines weichen Nebels zu erzeugen. (Lustige Tatsache: Es gibt 120.000 Vibrationen in einer Sekunde!). Das Gerät ist atemaktiviert und es dauert nur ein paar Atemzüge, um den Insulinnebel Dance 501 einzuatmen. Ein grünes Licht zeigt an, dass Sie den Nebel entsprechend einatmen, bevor ein blaues Licht am Gerät blinkt, um anzuzeigen, dass Sie fertig sind. Whitaker sagt, dass sie der FDA kürzlich ihre Designempfehlungen für das erste Gerät gesendet haben und erwarten, dass sie Anfang November behördliches Feedback erhalten.
Inhalationsgerät der nächsten Generation: Während die erste Generation ein Paar AA-Batterien verwendet, wird sich dies laut Whitaker wahrscheinlich bereits sechs Monate nach dem Start mit einem wiederaufladbaren Gerät der zweiten Generation ändern. Dadurch werden Größe und Gewicht des Geräts um 50% reduziert, sodass es eher wie eine Chanel-Lippenstift-Tube aussieht.
Schnelleres Handeln: Whitaker sagt, dass Dance 501 schneller wirkt als herkömmliche Insuline (speziell Humalog) und das inhalierte Insulin von Afrezza verbessert, da die Insulinwirkung genauso schnell ihren Höhepunkt erreicht, aber einen „längeren Schwanz“ hat, der die natürliche Reaktion des Körpers ohne a genauer nachahmt Notwendigkeit für Follow-up-Dosen. Phase-II-Studien zeigen nur wenige Hypos und sehr wenig Husten bei Personen, die diesen inhalierten Insulinnebel verwenden, der natürlicher in die Lunge gelangt, ohne den Hals zu reizen.

Datenverfolgung und Konnektivität: Da es sich bei dem Inhalationsgerät im Grunde genommen um einen kleinen Computer handelt, zeichnet es Insulinverbrauchsdaten auf, wie z. B. Dosierungsmengen bei Einnahme, Inhalationsrate, Insulindosierungsmengen und wie viel Nebel tatsächlich in die Lunge gelangt, basierend auf der Atemtiefe. Dance plant außerdem die Einführung einer mobilen App für das Smartphone mit denselben Daten, die Patienten zusammen mit Gesundheitsdienstleistern anzeigen und schließlich mit anderen D-Geräten wie CGMs und Datenplattformen verbinden können. All dies ist einzigartig, da andere inhalative Insulingeräte bisher weder Tracking noch Gerätekonnektivität angeboten haben.
F & E-Timing: So aufregend Dance 501 auch sein mag, Geduld wird hier eine Tugend sein ... wir reden mindestens ein paar Jahre, wenn nicht länger. Dance hat in den letzten Jahren frühe klinische Forschungsergebnisse veröffentlicht. Dies wird mit Phase-II-Studien fortgesetzt, die voraussichtlich Mitte 2019 durchgeführt werden. Von dort aus gehen sie davon aus, dass sie im späten Stadium der Phase-III-Studien im Jahr 2020 beginnen und voraussichtlich bis Ende des Jahres den Zulassungspunkt erreichen werden. Natürlich ist die Finanzierung der Schlüssel zu all dem, daher kann der Zeitpunkt davon abhängen, was auch immer die Forschung zeigt und was die Aufsichtsbehörden letztendlich sagen.
Preisgestaltung: Whitaker sagt auch, dass sie immer noch Preis und Kosten untersuchen. Sie glaubt nicht, dass Dance 501 "heute ein Ausreißer für bestehende Insuline" sein wird, aber wenn sie global statt nur in den USA eingesetzt wird, kann dies dazu beitragen, die Preise für Patienten auszugleichen. Natürlich planen sie auch, mit den Zahlern zusammenzuarbeiten, bevor sie auf den Markt kommen.
Auch flüssige Formulierung: Nur weil Dance diese Nebelform von inhaliertem Insulin entwickelt, heißt das nicht, dass sie nicht auch eine flüssige Version für die Verwendung in einer Durchstechflasche / Spritze, einem Stift oder einer Insulinpumpe suchen, ähnlich der Whitaker sagt, dass traditionelle Marken jetzt auf dem Markt sind.
Sehr aufregend, aber natürlich können wir ungeduldigen Patienten nicht anders, als uns zu fragen: Was zum Teufel hat so lange gebraucht, um an diesen Punkt zu gelangen, und warum sind wir noch Jahre davon entfernt, dieses Produkt von Dance zu sehen?
Es gibt viele bewegliche Teile, die in unserem Chat mit Whitaker gut erklärt wurden.
Hinter den Kulissen mit Anne Whitaker, CEO von Dance Biopharm

Whitaker hat mit mehr als einem Vierteljahrhundert einen guten Lebenslauf in der Pharma-, Biowissenschafts- und Biotech-Industrie - von Diabetes über Onkologie, Herz-Kreislauf-, Atemwegs- und Gastroenterologie. Ihr Hintergrund umfasst die Präsidentin und CEO von KNOW Bio, Novoclem Pharmaceuticals, Inc. und Synta Pharmaceuticals, Inc. Vor allem für unsere D-Community ist natürlich ihre Zeit als Präsidentin der nordamerikanischen Region für Sanofi von 2011 bis 2014 Sie war verantwortlich für alle Geschäftsbereiche Pharma, Geräte und Verbrauchergesundheit.
Während dieser drei Jahre bei Sanofi, so Whitaker, habe das Unternehmen versucht, den Insulinkonsum mit Lantus voranzutreiben, und sich hauptsächlich darauf konzentriert, PWDs (Menschen mit Diabetes) dazu zu bringen, ihre Rezepte tatsächlich aufzunehmen und die Medikamente angemessen zu verwenden. Sie sagt, dass nur 30% ihrer zuvor nicht insulinabhängigen T2-Patienten ihre Rezepte aufgrund von Angst und Verwirrung hinsichtlich des Insulinkonsums erhalten haben.
Sie wusste bereits während ihrer Zeit bei Sanofi über Dance Bescheid und führte eine vollständige Unternehmensüberprüfung durch, als der Pharmariese sich auf den Eintritt in den Inhalationsinsulinmarkt vorbereitete. Whitaker merkt an, dass Sanofi sich für eine Partnerschaft mit MannKind (Hersteller von Afrezza) entschieden hat, weil es eine „unmittelbare Gelegenheit“ gab, ein Produkt schneller auf den Markt zu bringen, als Dance es könnte. Dies wurde als eine großartige Möglichkeit angesehen, den Insulinkonsum von injizierbaren Substanzen wegzulenken, erklärt sie. Sie sagt jedoch, dass das Unternehmen Afrezza nicht so kommerzialisiert hat, wie es sein sollte, um eine stärkere Präsenz für PWDs zu erreichen, und sie verließ Sanofi 2014.
Der ehemalige Sanofi Exec sagt: "Ich war frustriert"
"Sie können ein Produkt nicht im Tertiärbereich auf den Markt bringen", sagte sie. „Ich war ehrlich gesagt frustriert, als ich es aus der Ferne beobachtete. Weil ich das Potenzial von inhaliertem Insulin gesehen habe. Aus diesem Grund wollte Dance jemanden mit dieser Kommerzialisierungserfahrung ansprechen. Wir müssen uns jetzt auf die kommerzielle Bereitschaft konzentrieren. Wir beginnen diesen Prozess jetzt und die gesamte Diabetes-Community wird mehr von uns hören, wenn wir uns auf den Start vorbereiten. "
Whitaker fügt hinzu, dass sie in Alabama mitten im südlichen „Diabetes-Gürtel“ aufgewachsen ist. Da sie auch eine Tante und einen Onkel hat, die mit Typ 2 leben, und ihr Schwiegervater an Diabetes leidet, hat sie die emotionale Achterbahnfahrt beobachtet, die PWDs verursachen ertragen, und wie Ärzte Insulin zu oft als Bedrohung für Menschen mit T2D verwenden.
"Ich hoffe, dass ich das ändern und den früheren Insulinkonsum vorantreiben kann, bevor sie diesen kontinuierlichen Rückgang ihrer Diabetes-Reise durchlaufen", sagt Whitaker. „Dance hat mit Dance 501 ein Produkt, das eine weitere Option bietet. Es ist sicherlich kein Ersatz für Pumpen oder Basalinsulin, aber es hat einen früheren Platz im Paradigma der Behandlung. "
Natürlich weiß Whitaker, dass es ein harter Kampf ist, Investoren und andere vom Potenzial von inhaliertem Insulin zu überzeugen. Sie glaubt jedoch, dass das, was sich in den letzten zehn Jahren geändert hat - nach dem Scheitern von Exubera, dem Start und Neustart von Afrezza durch MannKind und der allgemeinen Entwicklung von Technologie und Verneblung weltweit - die Bühne für Dance 501 auf eine Weise bereitet hat, die vorher nicht möglich war .
Tanzgründer John Patton war Mitbegründer und Chief Science Officer von Nektar Therapeutics, das die wissenschaftliche Grundlage für Exubera bildete, und er bleibt Teil von Dance, jetzt mit einem Sitz im Board of Directors. Eine weitere Führungskraft, mit der wir 2011 gesprochen haben, ist Samantha Miller, die weiterhin eine strategische Beraterin für das Unternehmen ist, das sich auf die Kommerzialisierung vorbereitet.
Interessanterweise, so Whitaker, hatte Dance Biopharm geplant, gegen Ende 2015 einen Börsengang (Börsengang) zu beantragen, aber als Sanofi MannKinds Afrezza fallen ließ, änderte sich dieser Plan. Stattdessen hat das Unternehmen klinische Studien vorangetrieben und sein Gerät so überarbeitet, dass es schlanker und anspruchsvoller ist.
Eine reife Umgebung für inhalierbare Stoffe
Die Zeiten haben sich sicherlich geändert - was Dance Grund zu der Annahme gibt, dass die Menschen offener für die Idee von Inhalationsmitteln sind.
Heutzutage sind E-Zigaretten und Vapes weltweit verbreitet, und Whitaker weist darauf hin, dass die medizinische Verneblung explodiert und weltweit mehr Akzeptanz findet. Sie zitiert, wie 8% des US-amerikanischen Medizinmarktes Handvernebler für Steroidmedikamente verwenden, verglichen mit 12% in Europa und 20% in China.
„Das Potenzial, Dance 501 erfolgreich auf den Markt zu bringen und zu vermarkten, ist vorhanden. Das Timing ist richtig für Dance “, sagt Whitaker.
Die Herstellungskosten sind sicherlich ein Problem für Whitaker, da er genau weiß, wie viel Exubera und Afrezza für die Herstellung und Markteinführung kosten - ab 1 Milliarde Dollar (!). Aber sie sagt, dass Dance nur einen Bruchteil dieser Kosten ausgeben kann. Sie arbeiten mit Asiens größtem Insulinhersteller zusammen, um von der FDA inspizierte Anlagen zur Herstellung von Dance 501 für die USA in Übersee zu haben.
"Wir haben auch das Glück, dass wir auf den Schultern des inhalierten Insulins stehen, das vor uns lag, denn es gibt jetzt eine Fülle von Daten über Sicherheit, Wirksamkeit und Patientennutzung, auf die wir zurückgreifen können", fügt sie hinzu.
Whitaker fügt hinzu, dass die Forschungs- und Fertigungsteams des Unternehmens in der Region San Francisco bleiben werden, während das kommerzielle Hauptquartier für Dance Biopharm innerhalb der nächsten 6 bis 9 Monate in den Research Triangle Park in North Carolina verlegt wird und bis dahin in Betrieb ist aus der Ferne. Sie planen auch, ein europäisches Büro sowie eines in China zu eröffnen, sagte sie.
Inhalatives Insulin gewinnt an Traktion?
Wir bleiben vorsichtig optimistisch hinsichtlich des Potenzials dieses neuen Produkts. Nehmen Sie als Beispiel MannKinds Afrezza: Wir beide hier im 'Bergwerk benutze es und liebe es. Tatsache ist jedoch, dass MannKind Probleme hat und ihre Verschreibungszahlen niedrig bleiben. Viele Ärzte zögern im Allgemeinen immer noch mit der Pulverformulierung, die seit 2015 auf dem Markt ist. Der Insulinmarkt ist wettbewerbsfähig und unbeständig, und nichts ist garantiert (außer der Tatsache dass wir PWDs mit T1D nicht ohne gehen können!).
Vor diesem Hintergrund hoffen wir jedoch, dass Dance es auf den Markt schafft und dort erfolgreich sein kann, wo Exubera versagt hat und MannKind Schwierigkeiten hat, Fuß zu fassen.
UPDATE: Im September 2019 wurde das Unternehmen in Aerami Therapeutics umbenannt.