Eine große Neuigkeit im Technologiebereich der Diabetes Community, da die FDA einem künftigen Closed-Loop-System, das einen kontinuierlichen Glukosemonitor mit einer Insulin-Patch-Pumpe kombiniert, die Bezeichnung „Durchbruch-Gerätebezeichnung“ erteilt hat, um mit dem schlauchlosen Omnipod mithalten zu können.
Am 14. März erteilte die FDA dem südkoreanischen Unternehmen EoFlow diese schnelle Bezeichnung für sein AID-System (Automated Insulin Delivery) namens EoPancreas. Dies ist das vierte Mal, dass die FDA einem neuen Diabetes-Closed-Loop-System seit seiner Einführung im Jahr 2016 die neue bahnbrechende Gerätebezeichnung erteilt hat. Bigfoot Biomedical erhielt sie im November 2017 für ihre zukünftige AID-Technologie, und Medtronic erhielt sie mit pädiatrischer Zulassung des Minimed 670G im vergangenen Sommer und dann wieder im Februar 2019 für ein zukünftiges „personalisiertes Closed-Loop-System“, das das Unternehmen entwickelt.
Obwohl EoFlow in diesem Bereich nicht so bekannt ist wie einige andere, ist es ein Unternehmen, das wir im Laufe der Jahre gesehen haben, wie es auf Konferenzen wie den jährlichen wissenschaftlichen Sitzungen der ADA seine Patch-Pumpe und die angeschlossene mobile App vorstellte. Die schlauchlose Pumpe selbst heißt EoPatch, und es wurde gemunkelt, dass sie an einem CGM arbeiteten, aber bisher waren nicht viele Details verfügbar. Das JDRF hat vor ein paar Jahren eine Partnerschaft mit dem Unternehmen geschlossen (das erste Mal, dass es eine koreanische Closed-Loop-Forschung finanzierte), und jetzt feiern sie den Zugang zu einem beschleunigten behördlichen Überprüfungsprozess, der zu einem früher als erwarteten Start hier in der EU führen könnte USA.
Folgendes wissen wir über die EoPancreas nach einem Gespräch mit EoFlows Präsident Luis Malave (einem ehemaligen Insulet-Manager vor über einem Jahrzehnt und Minimeds F & E-Direktor in den 90er Jahren) sowie Online-Informationen:
Was ist EoPancreas?

Für diejenigen, die noch nie von EoFlow gehört haben, ist es ein 2011 gegründetes südkoreanisches Unternehmen, das jetzt ein Büro in San Jose, CA, hat. Sein Gründer und CEO Jesse Kim leitete nach seinem Abschluss am MIT ein Halbleiter-Startup im Silicon Valley und gründete schließlich EoFlow als Inkubationszentrum für Universitäten in Seoul. Seit Oktober 2017 ist Malave Teil des Teams, das im kalifornischen Büro arbeitet.
Die Produktreihe, aus der das EoPancreas-System besteht, umfasst jetzt:
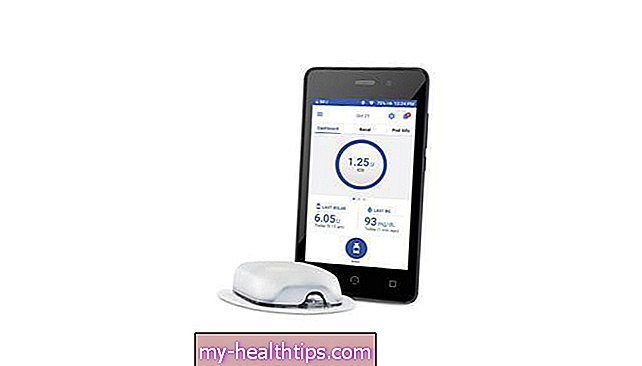
Patch-Pumpe: Als EoPatch bezeichnet, handelt es sich um eine rechteckige Insulinpumpe in Pager-Größe, die auf der Haut haftet, ohne dass Kunststoffschläuche erforderlich sind, wie dies bei herkömmlichen Pumpen der Fall ist. Es ist vollständig wegwerfbar und wasserdicht, hält 72 Stunden am Körper und fasst bis zu 200 Einheiten Insulin. Das Design, das letztendlich auf den Markt kommt, kann bis zu einem gewissen Grad variieren, aber der Formfaktor bleibt größtenteils gleich. Die vorhandene EoFlow-Patchpumpe der ersten Generation ist mit 9,9 mm x 32,4 mm x 12,9 mm deutlich dünner als der OmniPod (39 mm x 52 mm x 14,5 mm). Das EoPatch verwendet außerdem eine 30-Gauge-Edelstahlnadel im Inneren, um Verstopfungen (Verstopfungen) zu minimieren. Da das CGM jedoch in die Patch-Pumpe selbst eingebaut werden würde, würde es wahrscheinlich etwas dicker werden, etwa einen halben Zentimeter. Malave sagt uns auch, dass sie erwarten, zuerst nur die Patch-Pumpe in den USA als eine Art erste Generation auf den Markt zu bringen, bevor sie intelligente Algorithmen und schließlich die eingebaute CGM-Technologie hinzufügen.
Empfänger- oder Smartphone-Steuerung: Die in Korea bereits verfügbare EoPatch-Version verwendet ein Handheld-Gerät, das dem Personal Diabetes Manager (PDM) von OmniPod ähnelt. Es gibt keine Tasten an der Patch-Pumpe. Laut der EoFlow-Website würde für das, was in Amerika auf den Markt kommt, ein spezieller Handheld-Controller mit farbiger Touchscreen-Oberfläche verwendet - ein gesperrter Android-Smartphone-Stil. Ob dieses Gerät im PDM-Stil mit dem vollständigen EoPancreas-System eingeführt wird, bleibt abzuwarten, da das Unternehmen wahrscheinlich die Steuerung von Smartphone-Apps mit den Aufsichtsbehörden bespricht. Dies ist bereits eine Diskussion, die Insulet mit den Regulierungsbehörden für seine OmniPod-Closed-Loop-Plattformen der nächsten Generation führt, sodass wir dort in Kürze einige Bewegungen sehen können.
CGM-Sensor: Es gibt nicht viele Details in der Öffentlichkeit, aber wir haben erfahren, dass die EoPancreas in die vorhandene CGM-Technologie integriert werden. Insbesondere hat das Unternehmen eine Vereinbarung zur Verwendung des CGM-Sensors CT-100B von POCTech aus China getroffen, den wir auf Konferenzen als „Ich auch“ -Produkt gesehen haben, das mit seinem „winzigen weichen“ 0,3-mm-Sensor prahlt und Genauigkeit. Dieser CGM-Sensor wird in die Patch-Pumpe eingebaut, obwohl Malave uns mitteilt, dass sie auch hoffen, mit anderen CGM-Herstellern zusammenzuarbeiten, um diese als Optionen für das EoPancreas-System zu haben. Wie bereits erwähnt, wird der POCTech CGM-Sensor das gesamte Gerätedesign etwas dicker machen, sagt Malave. Angesichts der neuen Bezeichnung „iCGM“ (Interoperable CGM) der FDA, die Dexcom G6 zuerst erteilt wurde, können wir uns vorstellen, wohin EoPancreas in Zukunft gehen möchte.
EoCloud: Wie die meisten verbundenen Systeme heutzutage wird das EoPancreas eine eigene Cloud-basierte Software anbieten, die EoCloud heißt. Hierbei werden KI-Algorithmen (Artificial Intelligence) verwendet, die auf einer proprietären Plattform ausgeführt werden, um die Berechnungen durchzuführen, die es ermöglichen, mehr über jeden Benutzer zu erfahren, und die Anpassung der Regelung für jede PWD (Person mit Diabetes) zu ermöglichen. Uns wurde mitgeteilt, dass die Smarts des Systems auf dem Algorithmus von TypeZero Technologies basieren werden, der 2018 vor der Übernahme des Unternehmens durch den CGM-Hersteller Dexcom lizenziert wurde.
EoFlow geht davon aus, dass in diesem Jahr weitere FDA-Diskussionen stattfinden werden, da kürzlich eine „bahnbrechende Gerätebezeichnung“ erteilt wurde. Klinische Studien finden im Jahr 2020 statt und werden voraussichtlich im Jahr 2021 kommerziell eingeführt.
"Unser Unternehmen hat eine Flugbahn, auf die wir uns freuen", sagte Malave DiabetesMine. "Menschen mögen es, nur eine Sache zu haben, die sie tragen müssen, und alles läuft über das Smartphone, auf das wir einfach nicht verzichten können. Es liegt an uns, den Technologen, ihnen das zu geben und sicherzustellen, dass sie die Möglichkeit haben, es so zu personalisieren, wie sie es wollen. "
FDA's "Breakthrough Device Designation"
Das FDA Breakthrough Devices Program gewährt Unternehmen mit vielversprechenden neuen Technologien für die Behandlung chronischer Krankheiten eine vorrangige Überprüfung. Den Teilnehmern wird eine vorrangige Überprüfung sowie „interaktive Kommunikation in Bezug auf Geräteentwicklung und Protokolle für klinische Studien bis hin zu Kommerzialisierungsentscheidungen“ gewährt. Diese neue Bezeichnung für „neuartige, innovative“ Geräte, die erst 2016 erstellt wurde, wurde ~ 110 Artikeln verliehen und führte zur Genehmigung von etwa 10 davon.
Im D-Bereich mag es nach Bigfoot Biomedical und Medtronic Diabetes überraschend erscheinen, dass ein wenig bekanntes koreanisches Unternehmen als nächstes diese Bezeichnung im Wettbewerb um die Markteinführung der „Artificial Pancreas“ -Technologie erhalten würde.
Um ehrlich zu sein, hat unser Team immer die Augen über EoFlow gerollt, wenn wir sie auf Konferenzen gesehen oder im Laufe der Jahre erwähnt haben. Aber der JDRF scheint vor ein paar Jahren der Kurve voraus gewesen zu sein, als die Organisation Anfang 2017 bekannt gab, dass sie einen Teil der Forschung von EoFlow finanzieren würde - das erste Mal, dass die T1D-Gruppe auch Geld hinter dieses spezielle Closed-Loop-Unternehmen steckte als erste für die Finanzierung eines in Korea ansässigen Unternehmens für Diabetes-Technologie.
"Tragbare Designs der nächsten Generation, die kleiner sind und benutzerzentriertes Design verwenden, werden Hindernisse beseitigen, die einige Menschen, insbesondere kleine Kinder, daran hindern, diese lebensrettenden und lebensverändernden Glukosemanagementgeräte zu verwenden", sagte der JDRF-Forschungswissenschaftler Dr. Jaime Giraldo damals.
Wie schnell ihre Produkte auf den Markt kommen, hängt weitgehend von den FDA-Diskussionen ab, selbst mit diesem besonderen Status als bahnbrechender Bezeichnung.
Wir haben die FDA um weitere Einzelheiten zu den Unternehmen im Zusammenhang mit Diabetes gebeten, die diese Bezeichnung erhalten haben. Uns wurde jedoch mitgeteilt, dass Informationen im Rahmen des Überprüfungsprozesses als vertraulich betrachtet werden und nicht weitergegeben werden, es sei denn, ein Unternehmen beschließt, diese Informationen zuerst weiterzugeben. Wie bereits erwähnt, hat die FDA die Bezeichnung bisher nur vier spezifischen Systemen mit geschlossenem Regelkreis erteilt:
- Bigfoot Biomedical erhielt die Bezeichnung im November 2017, obwohl es zu diesem Zeitpunkt noch als „Expedited Access Pathway“ bekannt war, bevor es in Breakthrough Device Designation umbenannt wurde.
- Medtronic erhielt es im Juni 2018 mit der Genehmigung seines Minimed 670G für Kinder zwischen 7 und 14 Jahren.
- Im Februar 2019 erhielt Medtronic erneut diese bahnbrechende Fast-Track-Auszeichnung für seine zukünftige Personalized Closed Loop-Technologie - etwas, das über das derzeitige System mit mehr Automatisierung und personalisierten Aspekten hinausgeht.
- EoFlow wird in die Liste der EoPancreas aufgenommen, die eine Überprüfung der Pipeline-Technologie des Unternehmens einschließlich der Patch-Pumpe selbst, einer ersten „intelligenten“ Version und schließlich des CGM-integrierten Closed-Loop-Systems umfasst.
Laut Malave von EoFlow kann das Unternehmen mit dieser behördlichen Kennzeichnung „klare Meilensteine für Design und Entwicklung“ bei der FDA festlegen, um „unsere Fähigkeit zur Kommerzialisierung dieser wichtigen neuen Technologie zu beschleunigen“.
Es ist wichtig zu wissen, dass das Erhalten dieser Bezeichnung keine Garantie dafür ist, dass die Technologie eines Unternehmens notwendigerweise schneller verfügbar wird. Die ETA ist keine einheitliche Zeitachse, da sie von der Technologie und den regulatorischen Diskussionen abhängt. Dies versetzt EoFlow jedoch sicher in eine bessere Position, um auf den erwarteten Start bis 2021 hinzuarbeiten.
Neue schlauchlose Insulinpumpen und geschlossene Kreisläufe
EoFlow ist sicherlich nicht der einzige Player, der ein neues Closed-Loop- / AID- / AP-System mit einer schlauchlosen „Patch-Pumpe“ entwickelt. Es befinden sich noch viele weitere in der Entwicklung, darunter:
DiabeLoop: Dieses französische Startup entwickelt seinen DGLB1, ein hybrides System mit geschlossenem Regelkreis, das ein CGM, eine Patch-Pumpe und ein gesperrtes Smartphone zur Steuerung miteinander verbindet. In der ersten Generation wird die mehrfarbige Kaleido-Hybrid-Patch-Schlauchpumpe verwendet, ein kleines Rechteck, das sowohl am Körper haftet als auch über kurze, traditionelle Schläuche verfügt, die an ein Infusionsset angeschlossen werden. Während die Kaleido-Pumpe über Tasten verfügt, mit denen direkt dosiert werden kann, wird die Closed-Loop-Version über ein gesperrtes Smartphone (Sony Xperia Z1) mit dem DiabeLoop-System verbunden und über eine Datenquelle vom Dexcom G6 CGM eingespeist Algorithmus, um Dosierungsentscheidungen zu treffen. Diabeloop arbeitet auch mit anderen Partnern zusammen, zu denen die CellNovo-Hybrid-Patch-Tube-Pumpe gehört, und könnte dieses Gerät später auch verwenden. (Sehen Sie hier unsere frühere Berichterstattung über DiabeLoop.)
OmniPod Horizon: Während wir höchstwahrscheinlich auch einen Start im Jahr 2021 planen, sind viele in der D-Community sehr gespannt auf dieses Produkt der nächsten Generation des OmniPod-Herstellers Insulet! Basierend auf der jetzt eingeführten OmniPod DASH-Plattform, die Bluetooth Low Energy integriert hat, wird der Horizon eine Patch-Pump-Version eines Closed-Loop-Systems sein. Für diese Technologie befinden sich noch Versuche in der Entwicklung.
Roche Solo: Die Leute hatten das Solo-Patch-Pump-Gerät, das Roche bereits 2010 erworben hatte, so gut wie aufgegeben. Obwohl das Gerät der ersten Generation bereits von der FDA zugelassen war, traf Roche Diagnostics vor Jahren die Entscheidung des Unternehmens, es nicht auf den Markt zu bringen, weil es dies nicht tat. Dazu gehört ein integriertes Blutzuckermessgerät, wie es OmniPod getan hat - eine kopfschüttelnde Entscheidung im Nachhinein. Es blieb jedoch in der Entwicklungspipeline des Unternehmens und im Jahr 2018 in Roche endlich brachte die Solo-Mikropumpe in Europa auf den Markt. Es ist ein dünnes kleines Einweggerät, das nur ein kleines bisschen größer als der OmniPod ist, aber insbesondere abnehmbar (!) Und mit integrierten Tasten direkt vom kleinen Solo-Patch-Pod selbst Bolus. Roche arbeitet auch an der Integration von CGM-Technologien wie dem implantierbaren Eversense-CGM und wird diesen Teil schließlich in der Entwicklung zu einem Teil seines eigenen geschlossenen Regelkreises machen. Wir haben noch nichts hier in den USA gesehen, aber das bedeutet nicht, dass das Unternehmen sich nicht darauf vorbereitet, es hier einzureichen.
Lilly Diabetes: Wir haben berichtet, dass Lilly an seiner eigenen Technologie arbeitet, einer Hybrid-Patch-Tubed-Pumpe, die einer runden Tabakdose ähnelt, die in Ihre Handfläche passt. Der Pharma Giant arbeitet mit Dexcom als CGM-Partner zusammen und entwickelt dieses angeschlossene Gerät, das als automatisiertes Insulinabgabesystem bezeichnet wird und „möglicherweise über Funktionen mit geschlossenem Regelkreis verfügt“. (siehe unsere frühere Berichterstattung hier)
Tandems "t: sport" MiniPump: In der zukünftigen Pipeline entwickelt Tandem Diabetes Care eine Mini-Pumpe, die insgesamt etwas kleiner ist und eine geringere Patronengröße als die normale t: slim-Pumpe aufweist. Die Bildschirmanzeige entfällt, da alle Daten direkt auf einem Smartphone angezeigt werden. Es handelt sich um ein Gerät zum Aufkleben am Körper, aber nicht um eine vollständige Patch-Pumpe, da immer noch ein kurzer 4-Zoll-Infusionsset-Anschluss (Mini-Schlauch) benötigt wird. Mitte 2017 konnten wir im Hauptquartier von Tandem in San Diego einen Prototyp dieser Minipumpe sehen und halten. Angesichts der aktuellen Basal-IQ- und kurzfristigen Control-IQ-Closed-Loop-Technologie von Tandem zum Jahresende wird diese zukünftige Minipumpe zweifellos dieselbe Art von Closed-Loop-Fähigkeit bieten.
SFC Fluidics: JDRF hat sich auch mit SFC Fluidics aus Arkansas zusammengetan, um ein Patch-Pump-Closed-Loop-System mit offenen Protokollen zu entwickeln. Bisher gibt es nicht viele Details, aber SFC sagt, dass es "eine voll funktionsfähige Patch-Pumpe entwickeln wird, die auf seiner eigenen Plattform arbeitet und sein Kommunikationsprotokoll veröffentlicht, damit zugelassene Geräte mit der Patch-Pumpe kommunizieren können".
Neben diesen in der Entwicklung befindlichen Patch-Pumpensystemen und denen in der Do-It-Yourself-Community #WeAreNotWaiting, die mit dem OmniPod ihre eigenen „gehackten“ Versionen erstellen, gibt es auch andere AID-Systeme mit herkömmlichen Schlauchinsulinpumpen, darunter Medtronic, Tandem Diabetes, und solche wie:
Bigfoot Loop and Inject: Das kalifornische Startup arbeitet an einem AID-System (Automated Insulin Delivery), das intern als Bigfoot Loop und Bigfoot Inject bezeichnet wird. Es basiert auf seiner Pumpenversion, die die erworbene Asante Snap-Pumpentechnologie sowie eine angeschlossene Technologie verwendet "Smart Insulin Pen."
iLet Bionic Pancreas: Von Boston aus befindet sich dieses Pankreas nun unter dem Dach des Startups Beta Bionics und wird ein Dual-Hormon-Setup für die Dosierung von Insulin und Glucagon verwenden. Das Unternehmen befindet sich bereits in der vierten Generation des Prototyps, von dem wir erfahren haben, dass er der kommerziellen Version, die voraussichtlich in den nächsten zwei bis drei Jahren auf den Markt kommen wird, sehr ähnlich sein wird.
Wir freuen uns, dass ALLE diese potenziellen Closed-Loop-Angebote - insbesondere die Patch-Pump-Sorten - den Patienten eine große Auswahl bieten. Herzlichen Glückwunsch an EoFlow für das Vertrauensvotum der FDA.
Darüber hinaus schätzen wir die Bereitschaft der FDA, Unternehmen zu beschleunigen, die diese Art von Technologie der nächsten Generation ermöglichen!